Menu
Signatera™ es una prueba personalizada de ADN tumoral circulante (ctDNA) utilizada principalmente para monitorear el cáncer en pacientes que ya han sido diagnosticados.
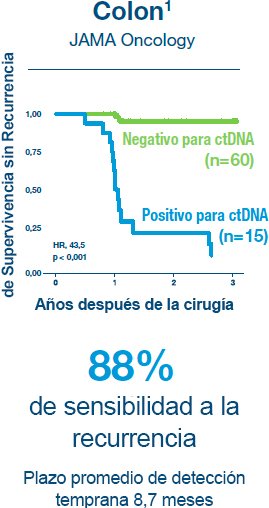
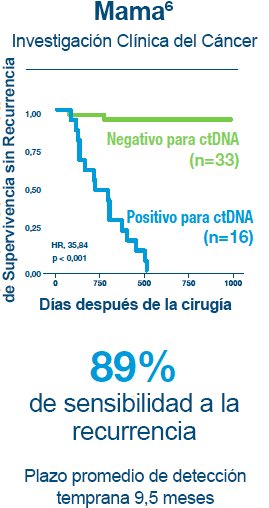
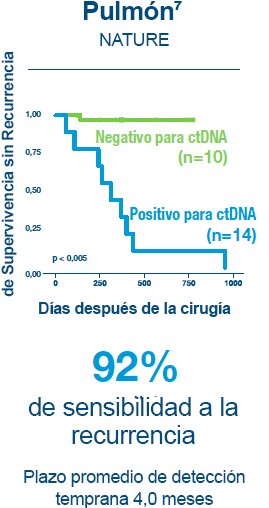

1. Reinert T, Henriksen TV, Christensen E, et al. Analysis of Plasma Cell-Free DNA by Ultradeep Sequencing in Patients With Stages I to III Colorectal Cancer. JAMA Oncol. 2019.
2. Sinicrope FA, Foster NR, Thibodeau SN, et al. DNA Mismatch Repair Status and Colon Cancer Recurrence and Survival in Clinical Trials of 5-Fluorouracil-Based Adjuvant Therapy. J Natl Cancer Inst. 2011;103(11):863-875.
3. Aoyama, Oba K, Honda M, et al. Impact of postoperative complications on the collorectal cancer survival and recurrence: analyses of pooled individual patients’ data from three large phase III randomized trials. Cancer Med. 2017;6(7):1573-1580.
4. Yothers G, O’Connell MJ, Lopatin M, et al. Validation of the 12-gene colon cancer recurrence score in NSABP C-07 as a predictor of recurrence in patients with stage II and III colon cancer treated with fluorouracil and leucovorin (FU/LV) and FU/LV plus oxaliplatin, J Clin Oncol. 2013;31(36):4512-4519.
5. Kotani D. et al., Molecular residual disease and efficacy of adjuvant chemotherapy in patients with colorectal cancer, Nature Medicine v29 Issue 1 Jan 2023
6. Coombes RC, Page K, Salari R, et al. Personalized Detection of Circulating Tumor DNA Antedates Breast Cancer Metastatic Recurrence. Clin Cancer Res. 2019;25(14):4255-4263.
7. Abbosh C, Birkbak NJ, Wilson GA, et al. Phylogenetic ctDNA analysis depicts early-stage lung cancer evolution. Nature. 2017;545(7655):446-451.
8. Christensen E, Birkenkamp-Demtroder K, Sethi H, et al. Early Detection of Metastatic Relapse and Monitoring of Therapeutic Efficacy by Ultra-Deep Sequencing of Plasma Cell-Free DNA in Patients With Urothelial Bladder Carcinoma. J Clin Oncol. 2019;37(18):1547-1557.
9. Data on file
10. Japanese Society of Medical Oncology Guidelines, October 2022.
Considere realizar esta prueba cuando haya:
Use Signatera™ en el contexto neoadyuvante para identificar y apoyar un enfoque de “observar y esperar” o no quirúrgico en determinados pacientes.
Use Signatera™ después de la cirugía para evaluar la necesidad de quimioterapia adyuvante y potencialmente evitar tratamientos innecesarios.
Use Signatera™ junto con pruebas CEA y de imagen para detectar la recurrencia más temprano.
Signatera™ permite el monitoreo en tiempo real de la dinámica de ctDNA para una evaluación temprana y sensible de la respuesta al tratamiento.
Exoma Tumoral
La metodología utilizada para este es:
Sangre: No requiere ayuno.
Biopsia: En Bloque de Parafina o Lámina.
Exoma Tumoral – Hasta 40 días naturales
Monitoreo – Hasta 12 días naturales
Solicitud médica.
Tipo | Descripción |
Técnica | ctDNA |
Precisión | Al rastrear solo variantes específicas del tumor, la sensibilidad se maximiza con un límite bajo de detección (LOD) del 0,01% de frecuencia alélica variante (VAF). Además, Signatera™ filtra la hematopoyesis clonal de mutaciones de potencial indeterminado (CHIP) para reducir significativamente los resultados falsos positivos. |

Oficina Principal
Rua Bento Gonçalves, 59, Sala 802 — Centro, Marau, RS — 99150-000
Oficina en Porto Alegre
Rua Gomes Jardim, 301, Sala 918/909 — Santana, Porto Alegre, RS — 90620-130